무세포 시스템에서 리보솜을 이용한 피리다지논 올리고머 합성

포스텍(POSTECH·총장 김무환) 이준구 화학공학과 교수 연구팀이 노스웨스턴대학, 텍사스대학 연구팀과 공동으로 파마코포어를 단백질 번역과정의 생화학적 반응을 통해 세포 밖에서 합성하는 새로운 사실을 밝혀냈다. 연구결과는 최근 국제학술지 '네이처 커뮤니케이션스'에 게재됐다.
리보솜은 수십억년간 세포 내에서 진화해 온 거대분자다. 전사된 mRNA를 인식하고 서열 정보에 부합하는 L-알파-아미노산을 순차적으로 중합해 단백질(또는 펩타이드)로 변환하는 분자 중합 기계이다. 최근 합성생물학 분야에서는 이런 리보솜의 중합 능력을 이용, 자연계에 존재하지 않는 비천연 아미노산의 중합 연구를 수행하고 있다.
연구팀은 비천연아미노산이 아닌 새로운 형태의 비천연 기질이 연속적으로 리보솜 내에 도입될 경우 현존하는 화학합성법으로 구현할 수 없는 고분자 중추구조의 구현이 가능할 것이라고 가정하고, 다양한 비천연 아미노산을 합성하고 세포 밖에서(무세포 시스템)에서 리보솜을 이용해 이들을 중합하려는 시도를 이어왔다.
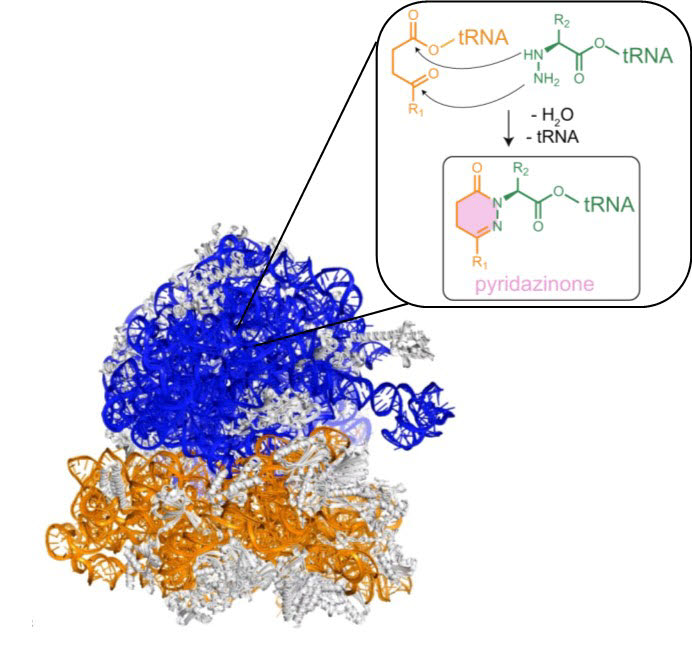
연구를 통해 '감마-케토산'과 '하이드라지노산'이 리보솜 내부에 연속적으로 도입되면 파마코포어로 자주 사용되는 '피리다지논(pyridazinone)'이라는 6각 고리형 구조가 형성되는 것을 확인했다. 나아가 6각 고리를 연속으로 도입, 고분자 형태 내 중추구조까지 형성하는 사실도 확인했다.
지금까지 연구에서는 리보솜 내부로 삽입된 아미노산 단량체들이 서로 중합반응을 거치면 단량체들끼리 서로 양팔을 벌려 악수하는 형태의 결합에 머물렀다면, 이번 연구에서는 아미노산이 아닌 새로운 형태의 비천연 단량체를 디자인해 단량체들끼리 고리형태로 연결된다는 것을 밝힌 것이다. 이는 리보솜을 이용한 단백질 합성과정이 단 한 가지 종류의 결합 방식(펩타이드 결합)으로만 이뤄진다는 사실을 뒤집는 혁신적 결과이다.

이준구 교수는 “단백질 번역과정에서 사용되는 다양한 생화학분자들이 오랜 진화과정에서 최적화돼 이를 조금이라도 변형하면 그 기능을 잃을 것이라는 일반적인 믿음과는 달리 의외로 수정 가능성이 크다는 것을 시사한다”며 “이러한 무세포 시스템이 앞으로 새로운 의약품 합성 기술뿐만 아니라 교대공중합체나 블럭공중합체의 합성 플랫폼으로 발전해 정밀 고분자, 특성 섬유의 생산으로 이어질 것을 기대한다“고 말했다.
이번 연구는 한국정부지원연구재단(NRF) 지원사업으로 진행됐다.
포항=정재훈기자 jhoon@etnews.com












































