#의료기기 업체 A사는 사우디아라비아 업체와 수출 계약을 맺었다. 공급 규모가 상당해 의미 있는 계약이었다. 기쁨은 오래가지 않았다. 예상치 못한 난관이 닥쳤다. 6개월이면 받을 줄 알았던 CE인증이 기약 없이 지연됐다. 수출 납기를 맞추지 못했고 결국 수출 계약은 취소됐다.
#레이저 치료기 업체 B사는 오는 9월 CE인증 만료를 앞두고 인증업체에 갱신을 신청했다. 하지만 수개월이 지난 지금까지도 감감무소식이다. 언제 가능할지 시점 예측은 고사하고 인증을 다시 받을 수 있을지도 알 수 없다. 이대로 가다가는 수출을 못할 것이 뻔하다. 문제를 해결하려 다른 인증업체에 의뢰했지만 불안감은 가시지 않는다.
국내 의료기기 업계에 CE인증 비상이 걸렸다. 2010년을 전후해 발생한 의료기기 사고로 절차가 강화되면서 인증이 지연되거나 취소되는 사례가 나타나는 등 후폭풍이 인다. 마땅한 대응책도 없어 기업은 발만 구르고 있다.
◇유럽 의료기기 스캔들로 ‘혼란’ 촉발
CE인증은 유럽 의료기기 판매에 필수다. 유럽연합(EU)은 의료기기 법(MDD 93/42/EEC)에 따라 1998년부터 CE마크를 부착한 의료기기만 유통케 했다.
의료기기 수출입 관리는 EU 각국 행정 당국에서 관장하며 서류 심사와 공장 심사 인증 업무는 국가별로 지정된 인증기관(NB:Notified Body)에서 담당한다.
인증기관 쪽에서 문제가 터졌다. 대형 의료기기 스캔들이 발생하면서 NB기관의 허술한 심사가 도마에 오른 것이다.
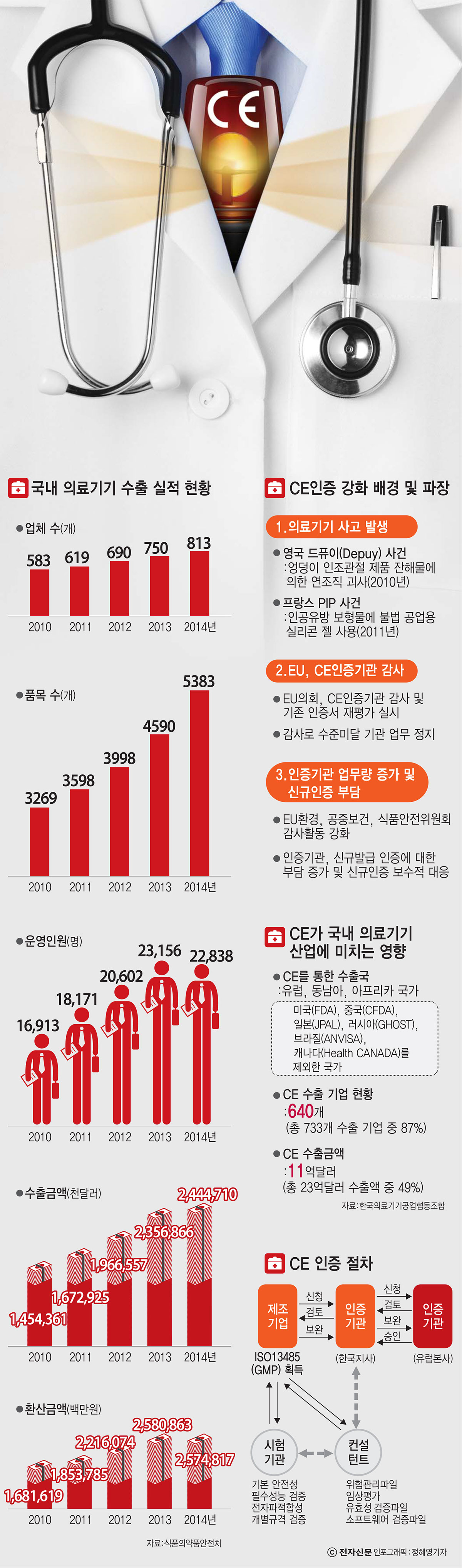
지난 2010년 발생한 영국 드퓨이(Depuy) 엉덩이 인조관절 제품에 따른 연조직 괴사 사건이 발단이다. 금속재질 고관절 치환술 후 제품 간 마찰로 생긴 잔해물이 연조직을 손상시키는 일이 발생, 파문을 낳았다.
2011년에는 프랑스 의료기기 업체 PIP가 문제를 일으켰다. 프랑스 여성 유방 확대용 실리콘 생산 업체인 PIP는 불법 공업용 실리콘 젤을 사용해 파문을 일으켰다. 문제의 보형물을 삽입한 여성 가운데 7500명은 보형물이 가슴 안에서 터졌다고 신고했고, 또 다른 수십명은 유방암에 걸린 것으로 알려져 사회문제가 됐다.
CE인증기관에 대대적 감사가 시작됐다. 발급 체계에 문제가 있다고 판단한 EU가 인증기관 전면 재검토에 나선 것이다. 파장은 거셌다. 감사로 수준미달 기관에 철퇴가 내려졌다. 다수 기관이 대거 업무 정지됐다. 한국의료기기공업협동조합 자체 조사에 따르면 EU 감사로 지난 2013년 100여개에 달하던 인증기관이 작년 80여개로, 또 현재 60여개로 감소했다. 인증기관 30%가 한꺼번에 문을 닫고 사라진 것이다.
◇영향권에 들어선 한국 의료기기 수출
인증기관 급감은 단순한 감소 이상 후폭풍을 불러왔다. 인증을 발급받고 싶어 하는 수요 대비 공급이 부족해지면서 인증 업무가 사실상 마비, 국내 의료기기 기업에도 직간접 영향을 미치기 시작한 것이다. 신규 인증 및 인증 갱신이 무기한 지연되는 사례, 또 기존 발급받은 인증이 인증기관 폐쇄로 취소되는 사례 등이다. 업계에 따르면 작년 하반기 피해 사례가 나타나기 시작했고 현재 여러 기업에서 실제 피해를 체감할 수 있는 수준에 이르렀다는 평가다.
의료기기 업체 C사 관계자는 “인증 갱신이 지연되면서 유럽에 납품하지 못하는 일이 발생했다”고 전했다.
이번 CE인증 문제로 인한 구체적 국내 산업계 피해 규모는 집계되지 않았다. 하지만 시간이 지날수록 피해 규모가 급증할 것이라는 게 중론이다.
실제로 우리나라 의료기기 수출 중에서 CE인증이 차지하는 비중은 가볍지 않다. 한국의료기기공업협동조합 분석에 따르면 국내 의료기기 수출액 23억달러(약 2조6000억원, 2013년 기준) 중 CE가 인정받는 국가에 수출한 금액이 11억달러(약 1조2500억원)에 달했다. 이는 의료기기 수출 중 절반 가까이 CE인증 영향을 받는다는 뜻으로 이번 CE인증 문제가 가져올 영향이 그만큼 크다는 분석이다.
박희병 의료기기조합 전무는 “CE인증은 단순히 유럽뿐만 아니라 동남아시아와 아프리카 국가 등에서도 인정받기 때문에 수출에 심각한 타격을 줄 수 있는 문제”라고 말했다.
인증 갱신을 기다리는 기업은 그나마 나은 편이다. EU 감사로 업무가 정지된 인증기관에서 CE를 받은 기업은 인증 자체가 취소돼 곧바로 판로가 막혔다. EU는 업무정지 기관에서 발급한 CE는 모두 말소시켰다. 다른 인증기관에서 전환심사를 받도록 돼 있지만 인증기관 부족으로 이 역시 원활하게 진행되지 않는다.
◇불을 끌 마땅한 수가 없다
유럽 CE인증 강화로 발등에 불이 떨어졌지만 난국을 돌파할 뾰족한 수가 보이지 않아 심각하다.
인증기관 자체가 줄어들었기 때문에 ‘급행’을 탈 수 있는 수단조차 없을 뿐더러 애초 인증을 강화한 배경이 안전한 의료기기를 확보한다는 데 있어 기준이나 심사 완화를 요구할 수도 없는 상황이다.
C사 관계자는 “조금이라도 심사 기간을 단축하고자 자료를 철저히 준비하는 것 외에 할 수 있는 일이 별로 없다”고 토로했다.
그나마 대기업이나 중견기업은 인허가 관련 업무를 전담해온 인력이 있어 정보 습득이 빠르고 변화에 대비하는 등 사정이 나은 편이지만 중소기업이 대부분인 의료기기 업계는 CE인증 문제로 직격탄을 맞을 수 있어 우려가 커진다.
윤건일기자 benyun@etnews.com