우리 연구진이 '항암제가 암세포를 죽이는 원리'를 밝혀냈다. 표적항암제가 세포 내 '단백질 공장'을 멈추고 스스로 죽게 만드는 것을 규명했다. 이 '자멸 과정'을 강화하면 약이 잘 듣지 않던 암세포도 죽일 수 있다.
한국과학기술원(KAIST·총장 이광형)은 임정훈 생명과학과 교수, 김동욱 의정부을지대병원 혈액암센터 교수, 김홍태 울산과학기술원(UNIST) 교수 공동연구팀이 만성골수성백혈병 항암제 반응을 조절하는 새로운 분자 기전을 규명했다고 23일 밝혔다.
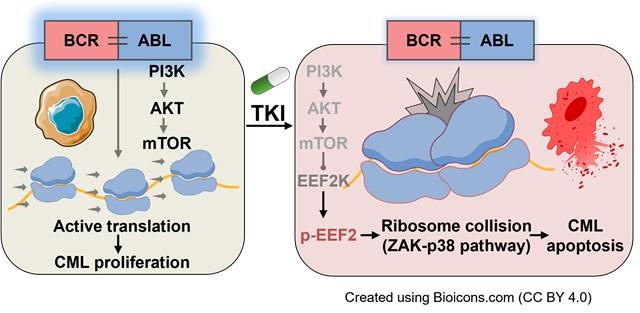
만성골수성백혈병은 조혈모세포에 유전적 이상으로 'BCR::ABL1'이라는 비정상 단백질이 만들어지며 발생한다. 이 단백질은 세포에 성장 신호를 보내 암세포를 계속 증식시키는 주 원인으로 알려져 있다. 이를 억제하는 표적항암제가 표준 치료로 쓰이지만, 일부 환자에서 약물 내성이 발생하거나 치료 반응이 낮다.
연구팀은 항암제가 세포 내 단백질 생산 과정에 미치는 영향에 주목했다. 그 결과, 항암제가 투입되면 단백질을 만드는 리보솜의 흐름이 꼬이면서 서로 부딪히는 '리보솜 충돌'이 발생한다. 세포 내에 강한 스트레스가 유발되고, 결국 암세포가 죽음에 이른다.
연구팀은 리보솜 충돌을 감지하는 핵심 센서로 'ZAK 단백질'을 지목했다. 이 단백질이 상황에 따라 '두 얼굴'을 가짐을 발견했다. 평소에는 AKT 신호와 결합해 암세포가 잘 자라도록 돕지만, 표적 항암제 치료가 시작되면 리보솜 충돌을 감시해 암세포 사멸을 이끄는 감시자로 돌변한다. 같은 단백질이 암 진행, 치료 과정에서 정반대 역할을 수행함을 세계 최초로 입증한 것이다.
이번 연구는 향후 표적항암제 효과를 높이고 새로운 병용 치료 전략 개발로 이어질 것으로 기대된다. 약물 내성으로 어려움을 겪는 환자에게 새로운 가능성을 제시할 전망이다.
임정훈 교수는 “이번 연구는 세포가 비정상적인 단백질 합성을 감지하고 이를 죽음의 신호로 전환하는 과정이 치료에 얼마나 중요한지를 보여준다”고 말했다. 제1 저자인 박주민 박사는 “리보솜 충돌이 암세포 사멸을 결정하는 핵심 스위치임을 확인한 만큼, 다양한 암종으로 연구를 확장해 나갈 계획”이라고 밝혔다.
이번 연구 결과는 '루케미아'에 3월 30일 온라인 게재됐다.
김영준 기자 kyj85@etnews.com












































