국내 연구진이 헤모글로빈 전환을 조절하는 핵심 단백질의 역할을 규명, 난치성 혈액 질환 극복을 위한 새로운 유전자 치료 전략을 제시했다.
한국연구재단은 전태훈 고려대 교수 연구팀이 적혈구 분화 과정에서 헤모글로빈 전환을 조절하는 핵심 단백질 LDB1의 역할을 규명했다고 23일 밝혔다.
헤모글로빈 전환은 태아기에서 성체기로 이어지는 적혈구 분화 과정 핵심 단계다. 전환이 제대로 이뤄지지 않으면 성체형 헤모글로빈 생성이 감소해 난치성 질환인 베타-지중해빈혈과 같은 유전성 빈혈이 발생한다.
이 전환을 조절하는 상위 조절 인자와 분자 기전이 그동안 완전히 밝혀지지 않아 유전성 빈혈 질환의 근본적 치료를 위한 분자적 표적을 제시하는 데 한계가 있었다.
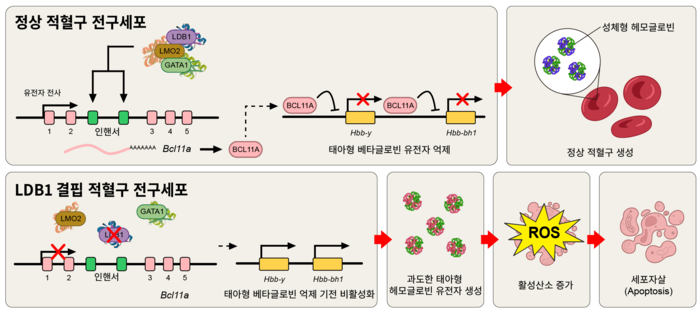
연구팀은 적혈구 전구세포에서 LDB1 단백질이 선택적으로 결핍된 생쥐 모델을 이용, LDB1이 태아형 헤모글로빈 억제 유전자의 발현을 직접 촉진하는 전사 활성화 인자로 작용한다는 사실을 밝혀냈다.
실험 결과 LDB1이 결핍된 적혈구 전구세포에서는 태아형 헤모글로빈 억제 유전자 발현이 감소하면서 태아형 헤모글로빈이 과도하게 생산됐다. 이 과정에서 활성산소가 증가하는데, 이는 적혈구 전구세포의 세포자살로 이어져 정상적인 적혈구 분화를 어렵게 한다.
실제 LDB1 단백질이 결핍된 생쥐는 적혈구 전구세포의 세포자살로 인해 심한 빈혈이 일어나고, 그로 인해 출생 후 일주일 이내에 사망하는 것으로 나타났다.
이 같은 결과는 LDB1이 산화 스트레스 조절과 적혈구 분화 유지에 필수적인 역할을 하며, 그 결핍이 베타-지중해빈혈에서 관찰되는 병태생리학적 현상과 유사한 조혈 장애를 유발함을 시사한다고 연구팀은 설명했다.
이번 연구는 적혈구 분화와 헤모글로빈 전환 메커니즘에 대한 이해를 한 단계 심화시킨 것으로, 향후 베타-지중해빈혈 및 사립체성 빈혈 등 산화 스트레스 관련 혈액 질환 치료 전략 개발에도 중요한 단초를 제공할 것으로 기대된다.
전태훈 교수는 “LDB1이 태아형에서 성체형으로의 헤모글로빈 전환을 주도하는 핵심 조절 인자임을 입증했다”며 “베타-지중해빈혈 유전자 치료제인 카스게비의 주요 표적 유전자(BCL11A)를 비롯한 헤모글로빈 전환 관련 핵심 유전자들을 함께 조절하는 LDB1의 기능은 베타-지중해빈혈에 대한 차세대 유전자 치료 전략으로 확장될 수 있다”고 말했다.
한편 이번 연구 성과는 생화학 및 분자생물학 분야 국제학술지 '리독스 바이올로지(Redox Biology)'에 지난 4일 온라인 게재됐다.
이인희 기자 leeih@etnews.com












































