
알츠하이머 치료제 레켐비가 출시된 가운데 국내 기업들의 치매 치료제 개발 현황도 주목받고 있다. 경구용부터 항체, 세포 치료 방식까지 다양한 접근법으로 치매 정복에 도전한다.
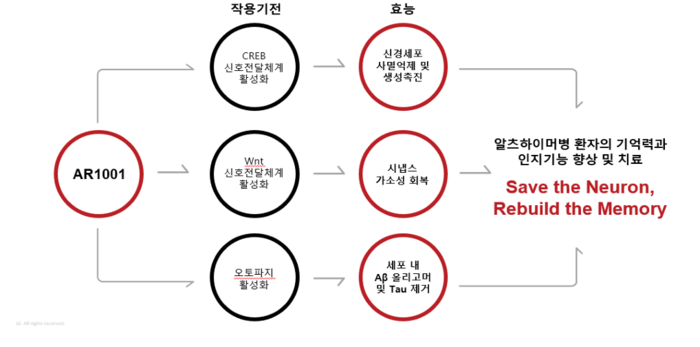
4일 업계에 다르면 아리바이오는 경구용 알츠하이머 치료제 'AR1001'을 미국, 유럽, 아시아 등 13개국에서 1150명을 대상으로 글로벌 임상 3상 진행 중이다. 3상에서 한국인 피험자를 100명 더 늘려 약 250명 규모로 확대했다. 한국내 임상시험센터도 21곳에서 26개로 5개 센터를 추가했다. AR1001은 독성 단백질 제거, 시냅스 활성화, 뇌 혈류 강화 등 다양한 작용으로 인지 기능 개선이 목표다.
아리바이오 관계자는 “빠르면 내년 말 임상 3상이 종료되고, 늦어도 2026년 초 마무리될 것”이라며 “데이터가 나오는 것에 따라 달라지겠지만 2026년 안에 미국 식품의약국(FDA)에 신약 신청을 할 수 있을 것으로 예상한다”고 말했다.
젬백스앤카엘은 알츠하이머 치료제 'GV1001' 국내 임상 2상과 미국과 유럽 7개국에서 글로벌 임상 2상을 진행 중이다. 미국 83명, 유럽 116명으로 총 199명의 환자 등록을 완료해 진행 중이다. 12개월 동안 피하 주사해 GV1001 유효성 및 안전성을 평가한다.
다중기전 약물인 GV1001은 2a상 임상 중 신경퇴행성질환으로 확장 가능성도 알렸다. GV1001은 세포 보호 효과, 신경 염증 감소, 각 세포 에너지원인 미토콘드리아 기능을 증가시키고, 신경 세포 이동성과 활동성을 향상시킨다는 설명이다. 삼성제약은 지난해 5월 젬백스앤카엘에서 알츠하이머병 치료제 GV1001의 국내 실시권을 취득했다.
네이처셀과 알바이오가 공동 운영하는 바이오스타줄기세포연구원은 자가지방유래 줄기세포를 척수강내와 정맥내로 병행투여해 알츠하이머 치매를 치료하는 재생의료 기술을 일본 후생성에서 승인받았다. 10월부터 도쿄 신주쿠클리닉에서 치료를 개시했다.
환자 자가지방에서 추출한 줄기세포를 배양한 후 정맥내 투여하거나 정맥과 척수강내 병용투여로 이뤄진다. 회당 2억셀에서 3억셀의 줄기세포를 2~6주 간격으로, 총 5~10회에 걸쳐 투여한다. 척수강내 시술은 줄기세포가 뇌와 척수로 직접 전달될 수 있다.
엔케이맥스는 미국 관계사 엔케이젠바이오텍이 자연살해세포(NK)를 활용한 세포 치료제 'SNK01'로 미국 임상 1·2a상을 진행하고 있다. 엔케이젠바이오텍 임상은 아밀로이드 베타와 함께 뇌 속 독성 단백질로 지목되는 타우 단백질 제거와 신경 염증을 감소시킨다.
지난 3월에는 미국에서 열린 알츠하이머치매 학회에서 멕시코 환자를 대상으로 한 임상 1상 추가 결과로 타우(Tau) 바이오마커 관련 세부 데이터를 발표했다. 정맥 투여한 SNK01은 뇌혈관장벽(BBB)을 통과하고, 뇌척수액(CSF)에 있는 알츠하이머 관련 바이오마커를 개선시켰다. 아밀로이드 베타, 타우, 알파-시누클레인 관련 지표가 개선됐다.
서울아산병원 윤승용 교수가 설립한 아델도 타우 단백질을 선택적으로 겨냥하는 항체 'ADEL-Y01' 미국 임상 1상을 진행 중이다. 아델도 알츠하이머협회 국제 콘퍼런스(AAIC)에 참가해 오스코텍과 공동개발 중인 타우항체(ADEL-Y01) 미국 임상 1상 디자인을 소개하고 연구 결과를 발표했다.
송혜영 기자 hybrid@etnews.com












































