유전자 발현과정 조절하는 'miRNA'
생성과정 알아내 질병원인 분석 도움
전구체 자를 때 고해상도 포착 성과
연구성과 2건 네이처 동시 게재
기초과학연구원(IBS·원장 노도영)은 김빛내리 RNA연구단장(서울대 생명과학부 석좌교수)팀이 RNA 유전자 치료제 개발에 새 가능성을 열 연구성과 2건을 네이처에 동시 게재했다고 22일 밝혔다.
'다이서 단백질' 작동원리를 밝히는 한편, 서울대 세포 및 거대분자 이미징 핵심연구지원센터 소속 노성훈 교수(생명과학부 교수)팀과 함께 다이서 3차원(3D) 구조를 최초 규명했다.
다이서 단백질은 드로셔 단백질과 함께 마이크로RNA(miRNA) 전구체를 절단해 miRNA를 만들어낸다. miRNA는 유전자 발현과정을 조절해 질병을 비롯한 모든 생명현상에 영향을 미친다. 전구체가 절단돼 miRNA가 만들어지는 과정을 알면 RNA 유전자 치료제 개발에 큰 도움이 된다.
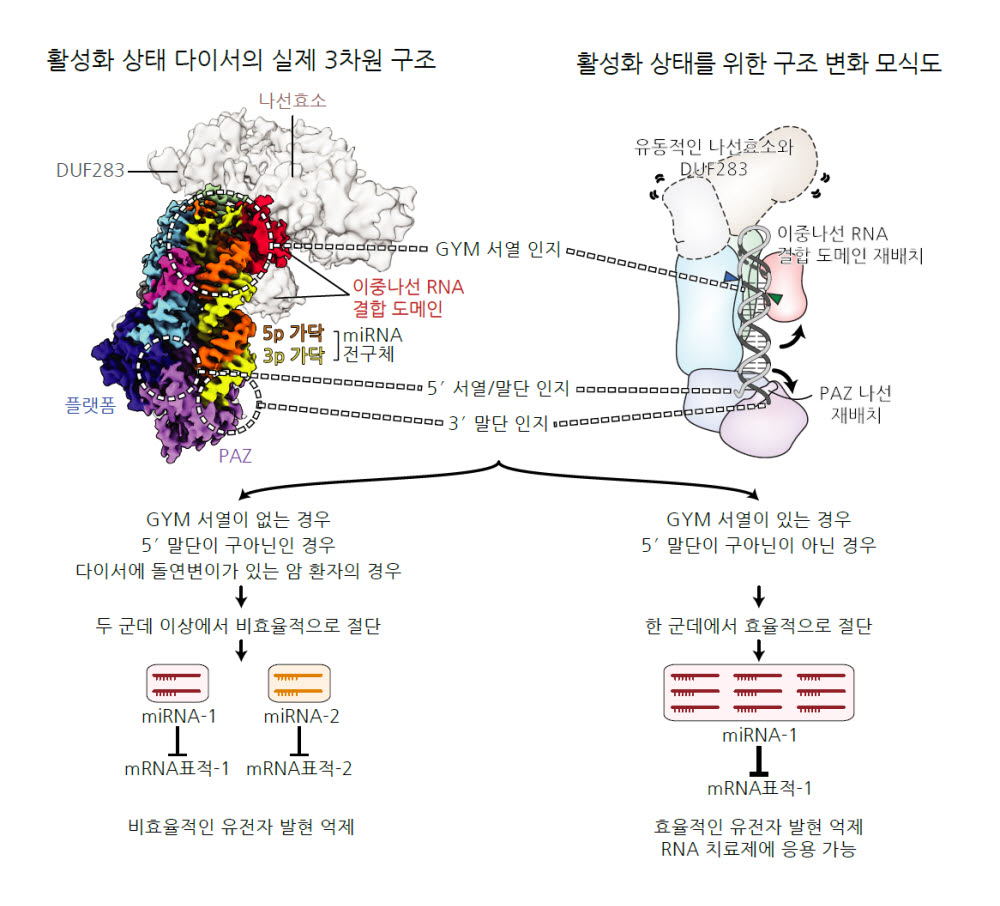
연구진은 RNA를 이루는 네 가지 염기인 구아닌·우라실·사이토신·아데닌이 무작위 구성된 miRNA 전구체를 100만종 넘게 합성한 후 이를 다이서로 한꺼번에 자르고 정량 조사했다. 이로써 다이서 전구체 절단에 필요한 'GYM 서열'을 발견했다.
연구진은 GYM 서열을 활용해 다이서가 miRNA 전구체 내 서열을 인지해 스스로 절단 위치를 결정함을 밝혔다. 또 유전자 발현과 질병을 억제하는 'RNA 간섭(RNAi)' 기법에 GYM 서열을 적용하면 그 효율을 높일 수 있다는 것도 확인했다.
노성훈 교수팀과 함께 사람의 다이서가 miRNA 전구체를 자르는 순간을 포착해 3D 구조를 고해상도 관찰한 것도 주요 성과다. 이는 더 효과적이니 RNA 치료제 개발을 가능하게 한다.
이들은 일부 암 환자의 다이서 특정 부분에 돌연변이가 발생한다는 것도 함께 발견했다.

김빛내리 단장은 “miRNA 생성과정을 이해하면 유전자 변이나 이상 발현으로 일어나는 질병원인을 찾고, RNA 간섭 효율을 높여 유전자 치료기술을 발전시킬 수 있다”면서 “miRNA 생성과정 이해를 한층 확장하고 국제 경쟁력을 이어갈 수 있게 됐다”고 말했다.
김영준기자 kyj85@etnews.com