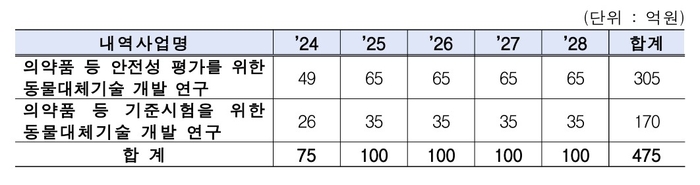
식약처, 2028년까지 475억 투입
오가노이드·생체조직칩 등
대체기술 표준화·시험법 개발
정부가 의약품 등의 상용화에 반드시 필요한 동물실험을 대체하는 오가노이드·생체조직칩 등 혁신 대체기술을 표준화하고, 동물대체시험법 개발 사업에 착수한다. 식품의약품안전처가 내년 추진하는 단일과제 중 최대 규모로 2028년까지 5년 동안 총 475억원을 투입한다.
식약처는 19일 서울 그랜드인터컨티넨탈 파르나스호텔에서 산학연 관계자 대상으로 설명회를 열고, 동물대체시험 표준화 사업을 내년부터 2028년까지 추진하겠다고 발표했다.

미국, 영국, 유럽 등 선진국은 동물실험을 금지하는 추세다. 미국은 오는 2035년부터 동물실험을 전면 중지할 예정이다. 지난해 말 조 바이든 대통령이 식품의약국 현대화법 2.0에 서명함에 따라 전임상 단계에서 동물실험을 대체하는 시험방법을 허용했다.
영국은 작년 동물실험실을 전면 폐쇄하고 오가노이드 등 대체시험법 개발 강화를 선언했다. 유럽의약품청(EMA)은 2016년 동물대체시험법 개발 프로젝트를 시작했고, 2019년에는 오가노이드 등 대체 모델 개발을 권장하고 있다.
오일웅 식약처 독성연구과장은 “그동안 각 부처가 오가노이드나 생체조직칩 등의 연구개발을 산발적으로 지원했으나 실제 현장 적용에 한계가 있었다”면서 “이번 사업으로 동물실험을 대체하는 표준 기술과 시험법을 확립해 국제 규제 변화에 대응할 계획”이라고 말했다.
지난 18일 열린 국회 보건복지위원회 법안소위에서는 동물대체시험법 활성화를 담은 2개 법안이 통과됐다. 식약처는 동물대체시험법을 의약품에 적용할 수 있는 법적 근거를 담은 '의약품 품목허가·신고·심사 규정'과 '의약품 임상시험 계획 승인에 관한 규정' 고시를 행정 예고해 내년 중 시행할 계획이다.
동물실험은 의약품 개발 시 독성 여부를 평가하는 전임상 단계에서 쥐·원숭이 등에 주로 이뤄진다. 동물은 실제 환자 상태와 완전히 동일하지 않아 인체 약물시험 반응을 정확히 예측하는 모델을 개발해야 신약개발 성공률을 높일 수 있다는 지적이 계속 제기돼왔다.
이번 사업에서는 심장, 신경계, 피부, 호흡기계, 신장, 소화기계 등에 걸쳐 오가노이드 등의 안전성·유효성 평가 시험법을 개발해 최적화한다. 또 시험계 품질보고서를 마련하고, 시험법 강점과 한계를 도출한다. 제브라피시·꼬마선충 등을 이용한 대체시험법 개발도 추진한다.
식약처는 오가노이드 표준화 연구를 지원하고 추후 동물대체자원은행을 구성할 계획이다. 각 병원·연구기관 등이 컨소시엄을 구축하고 웹에서 보유한 자원을 확인해 사용을 신청할 수 있는 바이오뱅킹 웹기반 인프라를 마련할 계획이다. 또 국내에서 개발한 동물대체시험법 국제 인증을 위해 OECD, ISO 등 독성시험 가이드라인 등재를 추진하고, 대체시험법 실용성을 높이도록 표준화 가이드라인을 마련해 보급할 계획이다.
인공지능(AI)을 활용해 오가노이드 안전성과 유효성, 품질 예측·평가에 활용하는 방안도 추진한다. 이를 기반으로 AI 기반 독성예측 모델을 산·학·연에 보급한다는 목표다.
배옥진 기자 withok@etnews.com












































