광주과학기술원(GIST)은 박한수 의생명공학과 교수가 조성엽 서울대 의과대학 교수팀과 공동으로 크리스퍼(CRISPR) 유전자 가위 기반의 유전체 스크리닝 플랫폼과 종양 마우스 모델 기반으로 신규 항암 표적인 TPST2를 발굴해 항암면역 조절 기전을 규명하고 TPST2 억제로 면역항암제의 치료 효능을 증가시킬 수 있음을 확인했다고 14일 밝혔다.
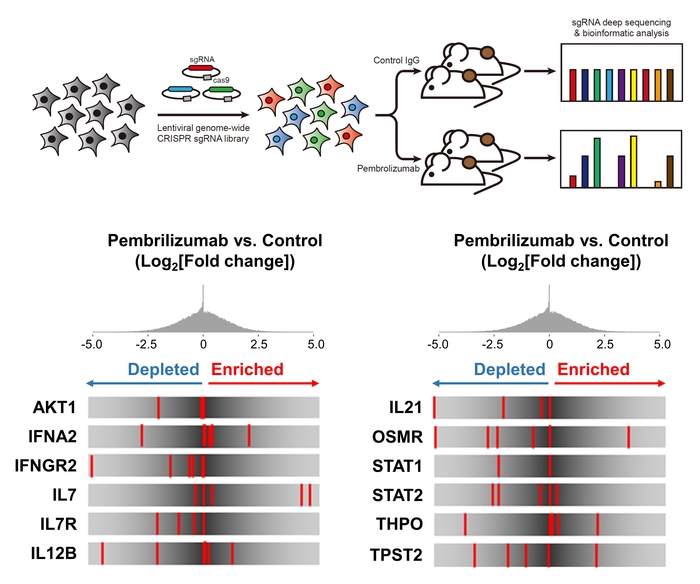
연구팀은 인간 유방암 세포주(MDA-MB-231)에 1만9050개 유전자를 표적하는 CRIPSR 라이브러리를 주입해 무작위적으로 유전자들이 제거되도록 했다. 이후 사람 유전자를 지닌 인간화 마우스에서 항-PD-1 치료를 병행해 생체 내 종양 성장의 변화를 확인했다. 대조군 종양 대비 항-PD-1 치료 종양에서 TPST2를 표적하는 sgRNA의 빈도가 감소한 것으로 나타났다. 이는 TPST2의 비활성화가 세포를 항-PD-1 치료에 더 민감하게 만든다는 것을 의미한다.
연구팀은 전사체 분석, 면역침전법, 질량분석법 등을 활용해 TPST2가 IFNGR1의 설포화를 진행해 면역을 조절한다는 기전을 규명했다. 종양 마우스 모델을 이용한 전임상시험에서 TPST2 제거만으로도 종양 성장을 유의미하게 억제하고 항-PD-1 치료 효과가 크게 향상됐다.

연구팀이 유세포분석법을 활용해 TPST2를 제거하자 종양 내 면역세포의 활성화가 유도되는 것을 확인할 수 있었다. 이를 통해 TPST2의 억제가 항-PD-1 치료의 면역 반응을 증대시켜 항암 효과를 극대화할 수 있다는 결론을 내렸다.
특히 다양한 임상 코호트를 분석해 여러 암종에서 정상 조직 대비 TPST2 유전자의 증폭 및 발현이 증가됐다. 유방암, 두경부암, 난소암, 육종, 위암, 자궁내막암 환자에서 TPST2 발현이 높은 경우 예후가 더 좋지 않았음을 확인했다. 이러한 결과는 TPST2 억제가 암 면역 치료에 중요한 역할을 할 수 있음을 시사한다.
생물학적 제제 제조기업 지놈앤컴퍼니 대표를 맡고 있는 박한수 교수는 “TPST2 억제제 개발을 통해 기존의 면역항암제에 불응하는 다양한 암환자를 대상으로 TPST2 바이오마커를 확인하고, 이에 따른 맞춤형 항암병용요법 치료 전략이 가능하다”고 말했다.
박 교수와 조 교수가 지도하고, 오유미 서울대 의대 연구원, 김수정·김윤재·김현 GIST 의생명공학과 학생 등이 함께 수행한 이번 연구는 한국신약개발사업단과 한국연구재단, 서울대학교 창의선도 신진연구자 과제, GIST 연구원 과제의 지원을 받아 이뤄졌다. 연구 결과는 암생물학 분야에서 가장 권위 있는 국제학술지로 평가받는 '분자 암(Molecular Cancer)' 온라인에 최근 게재됐다.
광주=김한식 기자 hskim@etnews.com












































