국내 연구진이 성장호르몬 과다 분비로 신체 말단이 커지는 만성질환인 말단비대증 연구를 위한 시험관 모델을 개발했다. 비수술적 약물 치료법 연구가 한 단계 발전할 것으로 예상된다.
광주과학기술원(GIST)은 오창명 의생명공학부·윤명한 신소재공학부 교수팀이 구철룡 세브란스병원 내분비내과 연구팀과 공동으로 말단비대증 연구를 위한 다공성 수화젤 섬유 기반 3차원(3D) 뇌하수체 종양모델 기술을 개발했다고 30일 밝혔다.
말단비대증은 외과적 처치를 통해 치료하는 경우가 많기 때문에 비수술적 약물 치료에 내성이 발생하는 원인을 규명하는 데 어려움이 있었다.
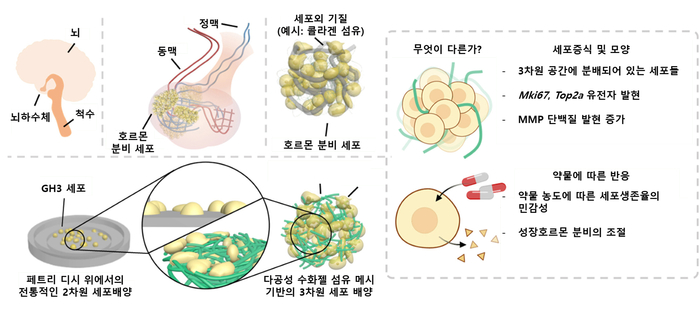
말단비대증에 대한 가장 일반적인 치료 방법은 수술로 종양을 제거하는 것으로, 그동안 성장호르몬 분비를 억제하는 약물 치료 방법인 소마토스타틴이나 소마토스타틴 유도체 투여 연구는 충분히 이뤄지지 않았다. 뇌하수체가 뇌 깊숙이 존재해 약물 내성이 발생하는 원인을 규명하는 데 한계가 있었기 때문이다. 성장호르몬을 분비하고 성장호르몬 분비를 억제하는 약물에 반응하는 시험관 수준에서의 뇌하수체 모델 개발이 필요한 상황이었다.
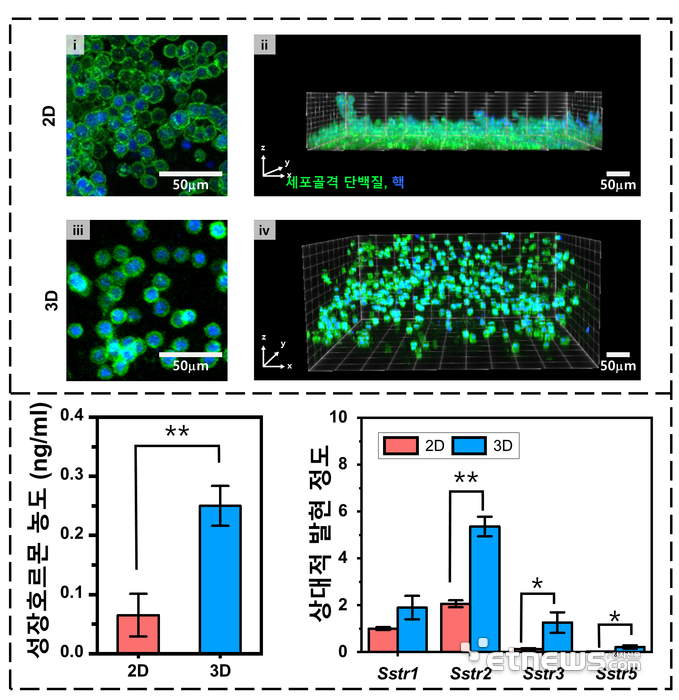
연구팀은 기존 뇌하수체 종양세포 모델이 실제 생체조직의 거동과 큰 차이를 보인다는 한계를 극복하기 위해 3D 구조를 갖는 다공성 수화젤 섬유에 종양세포를 배양했다. 이 모델에 약물 처리 시 성장호르몬 분비 억제와 세포 사멸 등이 기존의 2D 세포배양 모델에서보다 더욱 민감하게 발생한다는 것을 확인했다.
3D 뇌하수체 종양모델은 실제 환자에 대한 약물 투여 대신 시험관 수준에서 약물 처리를 통해 성장호르몬의 분비를 제어할 수 있다는 장점이 있다.
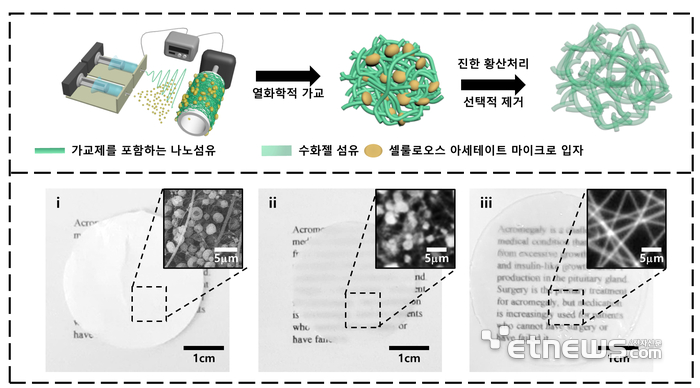
연구팀은 마우스 모델에서 유래한 뇌하수체 종양 세포인 GH3 세포를 기반으로 연구를 진행했다. 기존 2D 세포배양에서는 GH3 세포가 부착성이 낮고 분열속도가 느려 실제 뇌하수체 조직을 모사하는 데 한계가 있어 이를 해결하기 위해 폴리비닐알콜(PVA) 기반 다공성 수화젤 섬유 메시를 3D 세포배양 지지체로 사용했다. PVA 나노섬유는 세포독성이 없으나 세포부착이 낮고 섬유 간의 간격이 좁아 세포가 통과하기 어렵다.
연구팀은 PVA 용액의 전기방사 과정에서 전기분무로 셀룰로오스 아세테이트 미세입자 형성 후 간단한 산처리를 거쳐 이를 선택적으로 제거함으로써 3D 수화젤 섬유 구조 내 공극을 획기적으로 증가시키면서도 PVA 섬유의 세포부착 능력을 크게 높였다. 소마토스타틴 유도체 처리 시 넓은 표면적으로 약효가 보다 빠르게 나타났다.
오창명 교수는 “그동안 수술 위주로 접근했던 말단비대증 치료를 위한 약물 치료의 예후를 예측하고 내성이 발생하는 기전을 이해하기 위한 가능성을 열었다”며 “향후 약물 스크리닝을 통한 신약 후보물질 발굴과 같은 후속 연구를 기대하고 있다”고 말했다.

윤명한 교수는 “이번 연구는 단순히 새로운 세포 배양 지지체를 개발하고 3차원으로 세포를 배양하는 것을 넘어서 약물 반응을 검증할 수 있는 실용적인 3D 종양 모델을 시험관 내에서 구현했다는 점에서 더 큰 의미가 있다”고 강조했다.
이번 연구는 두 교수가 지도하고 정우주 석사과정생(현 프레스티지 바이오파마 아이디씨 연구원)과 왕성록 박사과정생(현 캘리포니아대 어바인캠퍼스 박사후 연구원)이 수행했으며, 구철룡 연세대 교수팀과 협력했다. GIST 생명의과학융합연구소 연구지원사업과 한국보건산업진흥원-아스트라제네카 당뇨연구지원 프로그램 지원도 받았다. 연구 결과는 스코푸스(SCOPUS)에 등재된 의공학 분야 상위 10% 국제학술지 '의학분야의 스마트 재료'에 최근 게재됐다.
광주=김한식 기자 hskim@etnews.com